Symphylans: Opciones para el control de plagas del suelo

Facilitado por:
Contenido
-
Introducción →
-
Daños →
-
Identificación →
-
Biología y Ecología →
-
Muestreo →
-
Gestión y control →
-
Referencias →
Compartir esta publicación
Por Jon Umble, Universidad Estatal de Oregón; Rex Dufour, NCAT; Glenn Fisher, Universidad Estatal de Oregón; James Fisher, USDA/ARS; Jim Leap, Universidad de California, Santa Cruz; Mark Van Horn, Universidad de California, Davis
Resumen
Los sinfílidos de jardín son organismos que viven en el suelo, parecidos a los ciempiés, que se alimentan de las raíces de las plantas y pueden causar daños importantes en los cultivos. Provocan problemas frecuentes y a menudo mal diagnosticados en suelos occidentales bien gestionados y con buena estructura. Es posible que esta plaga del suelo no resulte familiar para los agricultores y los asesores agrícolas. Esta publicación describe el ciclo de vida de los sinfílidos de jardín y los daños que pueden causar. Incluye técnicas de seguimiento para determinar si hay sinfílidos presentes en el suelo y opciones de gestión sostenible para prevenir daños económicos.
Introducción

Los suelos con un alto contenido en materia orgánica, una buena estructura y una reducid
e de perturbaciones, como en estos parterres excavados a mano, constituyen el hábitat ideal para los sinfílidos de jardín.
Los sinfílidos de jardín (Scutigerella immaculata Newport) son pequeños artrópodos del suelo, de color blanco y con aspecto de ciempiés, comunes en muchos sistemas de producción agrícola de Oregón, Washington y California (Berry y Robinson, 1974; Michelbacher, 1935).
Se alimentan de raíces y otras partes subterráneas de las plantas, lo que en algunos casos provoca pérdidas significativas en los cultivos. Su control puede resultar extremadamente difícil debido al movimiento vertical de los sinfílidos en el suelo, a la complejidad del muestreo y a la falta de métodos de control sencillos y eficaces (Umble y Fisher, 2003a).
Con la reciente expansión de la agricultura ecológica y la mejora de las técnicas de gestión del suelo, los daños en los cultivos asociados a los sinfílidos se han vuelto más habituales. Resulta irónico que estas plagas supongan un problema tan grave en explotaciones agrícolas que practican una buena gestión del suelo —manteniendo un suelo con buena estructura, alto contenido en materia orgánica y baja compactación—.
Daños
A veces resulta difícil diagnosticar un problema causado por los sinfilanos de jardín, ya que los daños pueden manifestarse de diversas formas y estos insectos no siempre son fáciles de detectar, incluso cuando los daños son evidentes. Los daños económicos pueden deberse a la alimentación directa de los cultivos de raíces y tubérculos, así como a la disminución de la densidad de los cultivos sembrados directamente o trasplantados (Umble y Fisher, 2003a).
Sin embargo, lo más habitual es que la alimentación de las raíces reduzca la capacidad del cultivo para absorber agua y nutrientes, lo que provoca un retraso general en el crecimiento. El daño en las raíces también puede hacer que las plantas sean más susceptibles a algunos patógenos vegetales transmitidos por el suelo. Para diagnosticar correctamente los problemas causados por los simfílidos en los
jardines e identificar las medidas de gestión adecuadas para un sistema de cultivo concreto, por lo general será necesario lo siguiente:
- Muestreo para determinar si los sinfílidos de jardín están presentes en cantidades que puedan causar daños
- Un conocimiento general de las estrategias de gestión y de la ecología de los simfílidos de jardín para seleccionar las estrategias específicas que resulten más eficaces en un sistema de cultivo determinado

Berenjenas con retraso en el crecimiento debido a los sinfílidos del huerto.

Berenjenas sin daños de la misma edad en el mismo campo.

Los daños causados por los sinfílidos pueden ser difíciles de diagnosticar, ya que pueden parecer debidos a otras causas. En esta foto se ven dos hileras de berenjenas: una con un retraso en el crecimiento muy marcado y otra en menor medida. Ni las hileras de la izquierda ni los pimientos de la derecha parecen estar afectados. Es probable que el momento de la siembra y del laboreo influya en la gravedad de los daños causados por los sinfílidos. Muchos factores pueden interactuar para favorecer o reducir el daño causado por los sinfilanos: las condiciones en las que se labra el suelo, el tiempo transcurrido tras la labranza, las necesidades térmicas del cultivo, la gestión del riego, el tamaño de la planta, etc.


Daños típicos y difíciles de identificar causados por los simfílidos: algunas hileras de pimientos (arriba, en la imagen superior) presentan un retraso grave en el crecimiento, mientras que en las hileras adyacentes hay plantas sanas y otras con retraso. Los daños causados por los simfílidos pueden confundirse con una siembra irregular o un mal contacto de la semilla con el suelo, como ocurre en estos campos de calabazas (arriba, en la imagen inferior), maíz dulce y tomates (abajo).



Algunas zonas de este campo de calabazas están devastadas por los sinfílidos, mientras que otras prosperan.

Daños típicos causados por los simfílidos, en los que se observan plantas sanas junto a plantas atrofiadas y zonas sin vegetación.
Identificación
Los sinfílidos de jardín no son insectos, sino miembros de la clase Symphyla. Las especies de esta clase son artrópodos del suelo muy comunes en todo el mundo. Los sinfílidos son pequeños animales blanquecinos parecidos a los ciempiés, cuyo tamaño oscila entre menos de 3 mm y unos 16 mm (o 6 mm en el caso de los sinfílidos de jardín) (Edwards, 1990). Tienen entre seis y doce pares de patas (dependiendo de la edad), lo que las hace fáciles de distinguir de los insectos comunes del suelo (por ejemplo, los colémbolos) y de los dipluros, que solo tienen tres pares de patas, todas situadas en el tórax o segmento medio del cuerpo.
Aunque su color puede variar en función de lo que hayan comido, los sinfílidos de jardín suelen ser más blancos y más pequeños que los ciempiés propiamente dichos, que también son artrópodos del suelo con muchos pares de patas (un par por segmento corporal) y movimientos rápidos. Los milpiés suelen moverse más lentamente y tienen dos pares de patas en cada segmento corporal.
Algunas especies de sinfilos se alimentan principalmente de materia orgánica muerta o en descomposición, desempeñando un papel importante en el ciclo de los nutrientes. Otras especies, como el sinfilo de jardín, son plagas graves, ya que se alimentan principalmente de plantas vivas.
En el oeste de Estados Unidos hay varias especies de Symphyla; sin embargo, el simfilo de jardín es la única especie de Symphyla de la que se tiene constancia que causa daños a los cultivos en esa zona. Los simfilos de jardín son, con diferencia, la especie de Symphyla más común en los sistemas agrícolas.
Si se detecta una alta densidad de sinfílidos en un sistema agrícola, concentrados alrededor de las raíces de las plantas, es probable que se trate de sinfílidos de jardín. No se tiene constancia de que esta plaga transmita ninguna enfermedad vegetal, aunque no se han llevado a cabo investigaciones exhaustivas al respecto.
Biología y ecología del Symphylan de jardín
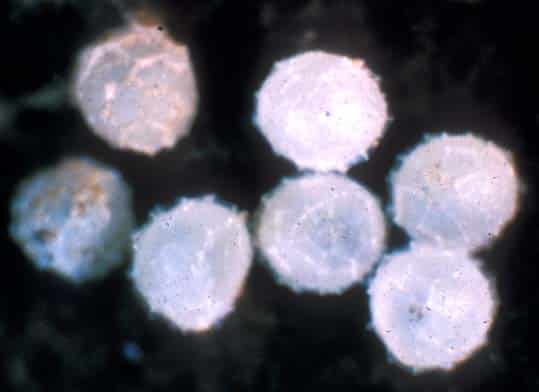
Huevos de simfílido de jardín. Foto: Ralph Berry
Ciclo de vida
En el oeste de Estados Unidos, los huevos, los adultos y los sinfílidos de jardín inmaduros pueden encontrarse juntos durante la mayor parte del año. La temperatura desempeña un papel fundamental en la regulación de la oviposición (puesta de huevos), y el mayor número de huevos suele depositarse en primavera y otoño (Berry, 1972).

Sinfílidos recién nacidos (primer estadio larvario). Crédito de la foto: Ralph Berry
Los huevos son de color blanco nacarado y esféricos, con estrías de forma hexagonal. La incubación dura entre 25 y 40 días cuando las temperaturas oscilan entre los 10 °C y los 21 °C, pero la eclosión se produce en unos 12 días cuando las temperaturas alcanzan los 25 °C (Berry, 1972).
Las primeras fases larvarias salen del huevo con seis pares de patas y seis segmentos antenales, y el cuerpo cubierto de finos pelos. Sus movimientos lentos y su parte posterior abultada hacen que, a simple vista, las primeras fases larvarias se parezcan más a un colémbolo que a un sinfilo de jardín adulto. Sin embargo, estas primeras fases larvarias rara vez se encuentran en la zona de raíces y, en cuestión de días, mudan a la segunda fase larvaria, que se asemeja a los sinfilos de jardín adultos de pequeño tamaño (Michelbacher, 1938).

Sinfílido adulto maduro de jardín.
Cada una de las seis mudas posteriores da lugar a la aparición de un par de patas y a un número variable de segmentos corporales y antenales. El tiempo total desde el huevo hasta el adulto sexualmente maduro (séptimo estadio) es de unos cinco meses a 10 °C, reduciéndose a unos tres meses a 21 °C y a menos de dos meses a 25 °C. Por lo tanto, es posible que haya dos generaciones completas al año (Berry, 1972). Curiosamente, a diferencia de los insectos adultos, que no mudan, los sinfílidos adultos de jardín pueden mudar más de 40 veces (Michelbacher, 1938).
Incidencia
El conocimiento sobre la presencia y el desplazamiento de los sinfílidos de jardín dista mucho de ser
completo. No obstante, se pueden establecer algunas generalizaciones tanto sobre los suelos en
los que los sinfílidos de jardín se dan con mayor frecuencia como sobre su desplazamiento en
los suelos. Las poblaciones de sinfílidos de jardín se concentran en gran medida dentro de los campos y
a mayor escala.

A menudo, los campos presentan daños causados por los sinfílidos en los mismos lugares a lo largo de varias temporadas, como ocurre en estas dos explotaciones.

En Oregón, Washington y California, los sinfílidos de jardín son más comunes en las regiones occidentales de estos estados. Dentro de estas regiones, suelen encontrarse en suelos más pesados y bien regados, y dentro de estos suelos, suelen concentrarse en «puntos calientes» que abarcan desde unos pocos metros cuadrados hasta varias hectáreas. Incluso en una sola palada de tierra, los sinfílidos de jardín suelen aparecer en agrupaciones muy bien diferenciadas.
Los sinfílidos de jardín no pueden excavar en el suelo. Utilizan poros, grietas estacionales y madrigueras excavadas por otros animales del suelo, como las lombrices, para desplazarse a través del perfil edáfico (Edwards, 1961).

Los poros, las grietas y los agujeros del suelo permiten a los sinfilanos
desplazarse por el campo con relativa facilidad.
En general, las prácticas que mejoran la estructura del suelo (por ejemplo, la incorporación de materia orgánica, la labranza reducida o los bancales elevados) mejoran la capacidad de los sinfílidos de jardín para desplazarse por el suelo, lo que da lugar a un aumento de las poblaciones y/o a un mayor daño debido a un mejor acceso a las raíces. Como resultado, las poblaciones elevadas de sinfílidos de jardín se encuentran con mayor frecuencia en suelos de textura fina y más pesados, con una estructura moderada o mejor y muchos macroporos, en lugar de en suelos arenosos (Edwards, 1958; Edwards, 1961). Cuando se encuentran sinfílidos de jardín en suelos más arenosos, estos suelos suelen haber sido enriquecidos con materia orgánica.
En el noroeste del Pacífico y el norte de California, los sinfílidos de jardín se encuentran habitualmente en suelos aluviales y es probable que su propagación se deba, en cierta medida, a las inundaciones. La acidez relativa del suelo no parece estar estrechamente relacionada con la presencia de sinfílidos de jardín, ya que estos se encuentran tanto en suelos muy ácidos (por ejemplo, donde crecen los arándanos) como en suelos bastante alcalinos (por ejemplo, con un pH superior a 8).

En esta vista aérea de un campo de brócoli se aprecian claramente los «puntos críticos» de infestación por el simfílano de jardín (
).



Arriba: Tres imágenes de un campo de brócoli en las que se aprecia el daño causado por los simfílidos.
Los focos de infestación en los campos afectados suelen mantenerse estables de un año a otro, con pocos cambios en las poblaciones y una propagación lateral mínima, posiblemente debido a las características físicas del suelo. Sin embargo, sí se producen cambios en los focos de infestación (Umble y Fisher, 2003c).
Movimiento de Symphylan en el suelo y factores que influyen los niveles de población
Si las condiciones del suelo son favorables, los sinfílidos de jardín pueden migrar desde la superficie del suelo hasta una profundidad de más de 90 centímetros. El perfil del suelo, incluidos los horizontes compactados o arenosos y los niveles freáticos elevados que pueden dificultar el movimiento, determina la profundidad a la que pueden migrar los sinfílidos de jardín. El momento en que se producen las migraciones verticales se debe principalmente a la interacción entre la humedad, la temperatura y los ciclos de alimentación regulados internamente (Edwards, 1959b). Es importante comprender de manera general estas interacciones, tanto para determinar el momento y la interpretación de los esfuerzos de muestreo como para seleccionar las tácticas de gestión.
Los sinfílidos de jardín suelen agruparse en los 15 cm superiores del suelo cuando este está húmedo y cálido, y se desplazan a capas más profundas cuando el suelo se vuelve muy seco o frío. En Oregón, Washington y California, los sinfílidos de jardín suelen encontrarse en la superficie del suelo desde marzo hasta noviembre, y las poblaciones más abundantes en la superficie se observan en mayo y junio. Los sinfílidos de jardín pueden encontrarse en la superficie del suelo cuando las condiciones son bastante cálidas (por ejemplo, cuando la temperatura del aire supera los 35 °C), si hay suficiente humedad y las raíces son superficiales o están ausentes. En los valles interiores más cálidos, los sinfílidos pueden ser más activos en primavera/principios de verano y en otoño, y su actividad en la superficie disminuye en julio, agosto y hasta septiembre.
Los sinfílidos de jardín migran hacia la superficie del suelo (la zona radicular) para alimentarse y, a continuación, regresan a los estratos más profundos para mudar, tal y como lo demuestra la gran cantidad de pieles mudadas que se observan en dichos estratos. Cuando los sinfílidos de jardín se alimentan vorazmente tras la muda, pueden adentrarse en la zona superficial del suelo incluso en condiciones generalmente desfavorables (por ejemplo, de calor y sequía). Dado que las migraciones no están sincronizadas, suele haber partes de la población presentes en toda la zona habitable del perfil del suelo (Edwards, 1959b). La presencia de sinfílidos de jardín en la superficie del suelo también puede verse influida por otras variables que impiden el movimiento, como la labranza y la compactación provocada por los neumáticos de los tractores.
Muestreo
El muestreo de los sinfílidos de jardín es extremadamente importante para identificar los daños, tomar decisiones de gestión fundamentadas y evaluar los efectos de dichas decisiones. Sin embargo, el muestreo suele resultar difícil. Se utilizan tres métodos principales de muestreo: el uso de cebos, el muestreo del suelo y el muestreo indirecto. Cada método tiene ventajas e inconvenientes, y la elección del método de muestreo variará en función de los objetivos del muestreo (por ejemplo, detección frente a estimación precisa de la densidad de población), la época del año y las condiciones del lugar.
Parte de la dificultad del muestreo se debe a la distribución irregular de las poblaciones. Es importante tener en cuenta que el recuento de una muestra concreta solo proporciona información sobre la zona cercana al lugar donde se tomó dicha muestra. Los recuentos suelen variar entre 0 y más de 50 sinfílidos de jardín por muestra. Para obtener información sobre los patrones espaciales de la población, lo mejor es tomar unidades de muestreo siguiendo un patrón de cuadrícula. Clasificar y comparar las muestras según factores del lugar, como el tipo de suelo, el drenaje y el historial de cultivos, puede proporcionar información valiosa sobre la distribución de las poblaciones dentro de un lugar.
Directrices generales para la toma de muestras
Para detectar o identificar un problema de sinfilanos en un cultivo en crecimiento:
- Por la mañana, desentierra las plantas raquíticas y las malas hierbas; examina sus raíces para ver si hay sinfilanos.
- Si han pasado unas tres semanas desde la siembra, coloca cebos para los sinfílidos del jardín en las zonas donde se sospeche que haya problemas.
Para calcular la densidad de población y/o tomar decisiones antes de sembrar un cultivo:
- Tome muestras de suelo si este está frío o muy seco, si el campo tiene muchas malas hierbas o si hay un cultivo de cobertura creciendo.
- Utilice el muestreo con cebo si el suelo está cálido y húmedo y presenta una vegetación escasa, o si el suelo está desnudo.
En la mayoría de los casos, el muestreo solo mide la densidad de sinfílidos en la capa superficial del suelo; por lo tanto, el muestreo solo debe realizarse cuando los sinfílidos de jardín se encuentran en la capa superficial del suelo. Las mejores condiciones para el muestreo son, por lo general, un suelo cálido y húmedo. El muestreo realizado en las tres semanas posteriores a una labranza importante —como el arado con disco, el arado tradicional o el laboreo con azada— suele ser inexacto, ya que es posible que los sinfílidos de jardín no hayan tenido tiempo suficiente para reestablecerse en la superficie del suelo. Si el muestreo se lleva a cabo poco después de la labranza, deben utilizarse métodos de muestreo del suelo. El muestreo debe realizarse a una profundidad que incluya varios centímetros de suelo no alterado por la labranza.
Muestreo del suelo
El muestreo del suelo es el método estándar e histórico para estimar la cantidad de sinfílidos de jardín presentes en un campo (es decir, el número aproximado de sinfílidos de jardín por unidad de suelo, o la densidad de población estimada) (Berry y Robinson, 1974). El tamaño de las unidades de muestreo varía. Las unidades de muestreo de suelo más habituales han sido las siguientes:
- Un cubo de 30 cm
- Un cuadrado de 15 cm de lado y 30 cm de profundidad
- «Una palada»
- Muestras de entre 7,6 y 10,2 cm de diámetro y entre 10 y 30,5 cm de profundidad

El muestreo del suelo en los cultivos de maíz se lleva a cabo colocando tierra sobre una lona negra y buscando con cuidado los sinfílidos de jardín.
Cuando se toman muestras de suelo, la tierra de cada unidad de muestreo se coloca normalmente sobre un trozo de plástico oscuro o de tela, donde se deshacen los agregados y se cuentan los sinfílidos de jardín (Berry y Robinson, 1974).
El muestreo debe realizarse a lo largo de toda la zona habitable del perfil del suelo (es decir, posiblemente hasta una profundidad superior a un metro) para obtener estimaciones precisas de la densidad de población, pero esto rara vez se lleva a cabo debido al gran volumen de tiempo y recursos que requiere. Por lo tanto, el muestreo se suele realizar cuando se cree que los sinfílidos de jardín se encuentran en las primeras 6 a 12 pulgadas de la zona radicular. El muestreo superficial (por ejemplo, hasta una profundidad de 4 pulgadas) ahorra tiempo y permite muestrear áreas más extensas, pero el muestreo más profundo (por ejemplo, hasta una profundidad de 12 pulgadas) suele ser más fiable. No se recomienda el muestreo en condiciones de mucha sequedad.
Muestreo de cebos
 En los últimos años se han desarrollado métodos de muestreo con cebos. Las muestras obtenidas con cebos suelen ser mucho más rápidas de tomar que las muestras de suelo, pero también son más variables y más sensibles a factores como la humedad del suelo, la temperatura y la presencia de vegetación (Umble y Fisher, 2003b). Para tomar una muestra con cebo, coloque media patata o remolacha en la superficie del suelo y cúbrala con una cubierta protectora (por ejemplo, una maceta blanca o una tapa de PVC de 10 cm).
En los últimos años se han desarrollado métodos de muestreo con cebos. Las muestras obtenidas con cebos suelen ser mucho más rápidas de tomar que las muestras de suelo, pero también son más variables y más sensibles a factores como la humedad del suelo, la temperatura y la presencia de vegetación (Umble y Fisher, 2003b). Para tomar una muestra con cebo, coloque media patata o remolacha en la superficie del suelo y cúbrala con una cubierta protectora (por ejemplo, una maceta blanca o una tapa de PVC de 10 cm).
 Entre uno y tres días después de colocarlos, retire los cebos y cuente, en primer lugar, los sinfílidos de jardín que se encuentren en el suelo y, en segundo lugar, los que estén en los cebos. En condiciones cálidas o secas, los cebos suelen revisarse entre uno y dos días después de colocarlos, ya que el número de ejemplares disminuye si se dejan al aire libre durante varios días. En condiciones más frescas, los cebos suelen dejarse al aire libre entre tres y cinco días.
Entre uno y tres días después de colocarlos, retire los cebos y cuente, en primer lugar, los sinfílidos de jardín que se encuentren en el suelo y, en segundo lugar, los que estén en los cebos. En condiciones cálidas o secas, los cebos suelen revisarse entre uno y dos días después de colocarlos, ya que el número de ejemplares disminuye si se dejan al aire libre durante varios días. En condiciones más frescas, los cebos suelen dejarse al aire libre entre tres y cinco días.

Fotos de arriba: Uso de un trozo de patata como cebo para detectar la presencia de sinfílidos en el jardín.
El muestreo con cebos funciona muy bien en algunas aplicaciones, aunque no se puede utilizar en todas las condiciones. El cebado da mejores resultados al menos dos o tres semanas después del laboreo, cuando el suelo se ha estabilizado, pero antes de que las plantas se hayan asentado bien. Si el desplazamiento hasta el lugar de muestreo requiere muchos recursos, puede ser preferible recurrir a métodos de muestreo del suelo, ya que solo exigen un único viaje al lugar.
Métodos de muestreo indirecto
El crecimiento de las plantas puede ser, en ocasiones, una medida indirecta útil de las poblaciones de sinfílidos en los jardines y suele constituir un buen punto de partida para evaluar sus patrones espaciales (Umble y Fisher, 2003a). Por ejemplo, las plantas sanas suelen indicar poblaciones bajas de sinfílidos en los jardines y, por el contrario, las plantas enfermas suelen indicar poblaciones elevadas de sinfílidos en los jardines.
¿Cuántas unidades de muestra de suelo o de murciélagos hay que utilizar?
A la hora de realizar muestreos de sinfílidos de jardín, se requiere un número crítico de unidades de muestra (es decir, «porciones» de tierra o cebos) para poder alcanzar un nivel razonable de confianza en la densidad de población estimada (por ejemplo, sinfílidos de jardín por pie cuadrado) (Umble y Fisher, 2003b). La confianza en esta estimación aumenta a medida que se toman más muestras. El muestreo implica establecer un equilibrio entre querer tener una certeza razonable sobre el número de sinfílidos de jardín presentes (tomando un gran número de muestras) y no invertir un tiempo y una energía excesivos en la tarea de muestreo (tomando un número reducido de muestras).
Siga estas pautas generales para determinar el número adecuado de unidades de muestra.
- Para detectar la presencia de sinfílidos en el jardín, puede que baste con desenterrar entre cinco y diez plantas dañadas o colocar un número reducido de cebos (por ejemplo, cinco).
- El muestreo en caso de densidades de población bajas (a principios de primavera o en cultivos muy susceptibles) requiere un mayor número de unidades de muestreo (por ejemplo, más de 100) que el muestreo en caso de densidades de población altas (por ejemplo, 30).
- A medida que aumenta la variabilidad de un método de muestreo, también lo hace el número de unidades de muestra necesarias. Dado que el método de cebos es más variable que el de muestreo del suelo, se necesitan entre dos y tres veces más cebos que muestras de suelo.
- Para estimar las densidades de población «perjudiciales desde el punto de vista económico» en cultivos moderadamente susceptibles, se suelen colocar al menos 35 unidades de muestreo de suelo o al menos 50 muestras de cebo. Dependiendo del tamaño del campo y de la época del año, se pueden utilizar muchas más unidades de muestreo.
Las medidas indirectas como esta pueden proporcionar información valiosa sobre el alcance y el patrón de la infestación, pero no deben utilizarse en sustitución del muestreo directo. Esto se debe a que hay muchos factores que pueden favorecer el crecimiento de plantas sanas, incluso en suelos infestados (por ejemplo, la fecha de siembra, la intensidad del laboreo, el uso de productos químicos y el tipo de cultivo).


Las plántulas de espinacas son susceptibles al daño causado por los sinfílidos. La tierra de la maceta de la foto superior contiene 45 sinfílidos. La tierra de la maceta de la foto inferior no contiene sinfílidos.
Umbrales de intervención: interpretación de los resultados del muestreo
Las decisiones de gestión, como las relativas a la aplicación de plaguicidas y la intensidad del laboreo, se basan a veces en estimaciones de la densidad de la población de sinfílidos de jardín realizadas antes de la siembra. Debido, en parte, a la gran variedad de cultivos en los que los sinfílidos de jardín actúan como plagas, los umbrales específicos para cada cultivo no están bien definidos. La relación entre las densidades de población de sinfílidos de jardín (estimadas mediante métodos de muestreo) y medidas como el recuento de plantas y el rendimiento se ve influida por factores como el tipo de cultivo, la intensidad del laboreo y la fase de desarrollo del cultivo (Umble y Fisher, 2003a).
En el laboratorio, se ha demostrado que concentraciones tan bajas como de entre cinco y quince sinfílidos de jardín por maceta reducen el crecimiento de las plántulas de cultivos como las judías verdes, las espinacas y el maíz dulce (Umble y Fisher, 2003a; Eltoum y Berry, 1985). Se ha demostrado que una densidad mayor, de 45 sinfílidos de jardín por maceta, reduce el crecimiento de las plántulas de tomate y espinaca en más de un 90 %.
En el campo, suelen producirse daños apreciables cuando la densidad de sinfílidos de jardín supera una media de entre 5 y 10 por palada en cultivos de susceptibilidad moderada a alta, como el brócoli, la calabaza, las espinacas y el repollo (Berry y Robinson, 1974; Umble y Fisher, 2003a).
En los sistemas de cultivo convencionales, se suele utilizar como umbral de tratamiento una población de entre dos y tres sinfílidos de jardín por pie cuadrado.
Debido a la considerable variabilidad de las densidades de sinfílidos en un campo, el recuento de individuos por muestra puede oscilar entre 0 y más de 100. Estos resultados resultan útiles para localizar los puntos críticos del campo. En cultivos más tolerantes, como la patata, las judías y los cereales de grano pequeño, la alimentación de los sinfílidos de jardín puede no provocar daños significativos, incluso con densidades de población considerablemente más altas (Umble y Fisher, 2003a).
Gestión y control
Son muchos los factores que influyen en los niveles de población de los sinfílidos de jardín (Howitt y Bullock, 1955; Umble y Fisher, 2003c; Getzin y Shanks, 1964; Shanks, 1966). Sin embargo, dado que resulta difícil realizar un muestreo preciso de las poblaciones, la información sobre los efectos reales de muchos de estos factores en los sinfílidos de jardín es, en el mejor de los casos, escasa. A efectos de gestión, es importante distinguir entre las tácticas que reducen las poblaciones y aquellas que reducen el daño a los cultivos, pero que no necesariamente reducen las poblaciones. En la mayoría de los casos, una gestión eficaz de los sinfílidos de jardín implica establecer un equilibrio entre estas dos estrategias. Es importante tener en cuenta que, en la mayoría de los casos, una vez que se detecta el daño, poco se puede hacer sin volver a plantar. Por lo tanto, el muestreo es importante para determinar el curso de acción adecuado.
Se desconoce si pueden desarrollarse poblaciones de sinfílidos a partir de tierra o compost transportados. Sin duda, estas son posibles fuentes de infestación, por lo que se recomienda tomar muestras de tierra y compost (tanto del propio terreno como de fuera de él) para detectar la presencia de sinfílidos antes de aplicar estos abonos al campo. En general, se considera que las poblaciones de sinfílidos son autóctonas y que se desarrollan con el tiempo gracias a unas prácticas de gestión del suelo adecuadas.
Estrategias para reducir las poblaciones
La reducción de las poblaciones ha sido el tema central de numerosos estudios (Howitt y Bullock, 1955; Umble y Fisher, 2003c; Getzin y Shanks, 1964; Shanks, 1966; Howitt, 1959; Peachey et al., 2002). Aunque no se ha identificado ninguna «solución milagrosa», existen algunas estrategias disponibles. Probablemente ningún método erradicará los sinfílidos de jardín de un lugar, y el efecto de la mayoría de las tácticas no durará más de uno a tres años.
Labranza
El laboreo es probablemente la técnica de control más antigua, y sigue siendo una de las más eficaces (Martin, 1948; Peachey et al., 2002). El laboreo puede aplastar físicamente a los sinfílidos de jardín, reduciendo así sus poblaciones. El laboreo también puede perjudicar a las poblaciones de depredadores clave de los sinfílidos de jardín, como los ciempiés y los ácaros depredadores. Sin embargo, en los sistemas de cultivo anual, no se ha demostrado que los beneficios del aumento de las poblaciones de depredadores derivado de la reducción del laboreo sean tan eficaces como el laboreo a la hora de reducir las poblaciones de sinfílidos de jardín. A la hora de plantearse aumentar el laboreo, los agricultores deben sopesar los beneficios y los costes, como la oxidación de la materia orgánica del suelo, la compactación del suelo y el aumento de los gastos en tiempo, combustible y desgaste de la maquinaria.
En general, para lograr un control más eficaz, se debe labrar el suelo cuando los sinfílidos del jardín se encuentran en la capa superficial y la humedad del suelo permite preparar un lecho de siembra fino. Dado que solo una parte de la población de sinfílidos se encuentra en la capa superficial, el laboreo nunca garantiza un control total. Sin embargo, las poblaciones superficiales suelen reducirse considerablemente durante al menos dos o tres semanas tras el laboreo.
Los sinfílidos de jardín son unos animales similares a los ciempiés que viven en el suelo, se alimentan de las raíces de las plantas y pueden causar daños importantes en los cultivos, que a menudo se diagnostican erróneamente. Se describe su ciclo de vida y las opciones de gestión sostenible.

Brócoli dañado (arriba) y sin daños (abajo) plantados al mismo tiempo en el mismo campo.


Pepinos dañados (arriba) y sin daños (abajo) plantados al mismo tiempo en el mismo campo.


Girasoles dañados (arriba) y sin daños (abajo) plantados al mismo tiempo en el mismo campo.


Pimientos dañados (arriba) y pimientos intactos (abajo) plantados al mismo tiempo en el mismo campo.

Pesticidas
En los últimos 100 años se han utilizado cientos de compuestos contra los sinfílidos de jardín, con distintos grados de eficacia (Howitt y Bullock, 1955). Los fumigantes y los plaguicidas organofosforados han sido los más eficaces, pero muchos de ellos
ya no están autorizados. Los plaguicidas pueden tener el efecto tanto de matar a los sinfílidos de jardín como de ahuyentarlos de la superficie del suelo. No se ha demostrado que los pesticidas menos tóxicos (por ejemplo, los piretroides y otros pesticidas naturales) proporcionen un control aceptable. Los pesticidas suelen ofrecer el mayor control cuando se aplican a voleo y se incorporan al suelo, aunque las aplicaciones en bandas e inyectadas pueden proporcionar un nivel de control aceptable.
Rotación de cultivos
Aunque los sinfílidos de jardín se alimentan de una amplia variedad de plantas, también pueden sobrevivir en suelo desnudo alimentándose de otros organismos del suelo. La susceptibilidad de las plantas a los sinfílidos de jardín varía enormemente. La rotación de cultivos puede explicar en parte los cambios aparentemente repentinos en los niveles de población de sinfílidos de jardín. Las poblaciones disminuyen significativamente en los cultivos de patata, lo que incluso permite el cultivo posterior de plantas susceptibles en la rotación (Umble y Fisher, 2003c). Aunque ningún otro cultivo
ha demostrado ser tan eficaz como la patata para reducir las poblaciones de sinfílidos, estas son más bajas tras un cultivo de cobertura de invierno de avena de primavera («Monida») que tras un cultivo de cobertura de invierno de mostaza («Martiginia»), cebada («Micah») o centeno («Wheeler») (Peachey et al., 2002). Los cultivos de mostaza y espinacas son muy buenos hospedadores y pueden provocar un aumento de las poblaciones en algunos casos. Todos estos factores deben tenerse en cuenta a la hora de elaborar un plan de gestión de malas hierbas.
Otros acondicionadores del suelo
Los efectos descritos de los enmiendas del suelo habituales, como el estiércol, la cal, los fertilizantes y el compost, varían enormemente y a menudo son contradictorios. En general, se acepta que la cal y los fertilizantes tienen poco efecto sobre las poblaciones, mientras que se cree que la aplicación de estiércol suele aumentarlas (Shanks, 1966). El efecto del compost y los acondicionadores orgánicos sobre las poblaciones de sinfílidos de jardín ha sido variable, pero hasta la fecha no se ha demostrado que ninguno de ellos reduzca de forma consistente y significativa las poblaciones de sinfílidos de jardín.
Estrategias para reducir los daños en los cultivos
La mayoría de las plantas pueden tolerar cierto nivel de alimentación por parte de los simfílidos de jardín durante toda o parte de la temporada de crecimiento, y existen dos estrategias generales que pueden ayudar a obtener cultivos sanos en suelos infestados de simfílidos. Estas estrategias consisten, por un lado, en reducir los daños a los cultivos cuando las poblaciones de simfílidos de jardín son elevadas y, por otro, en reducir el número de simfílidos de jardín en las raíces de los cultivos durante la fase de establecimiento, momento en el que las plantas suelen ser más vulnerables.
Estrategias para reducir los daños en los cultivos cuando las poblaciones de simfílidos en el huerto son elevadas

Patatas plantadas bajo el brócoli en la granja estudiantil de la UC Davis.

Patatas plantadas entre hileras de maíz dulce en un ensayo de cultivos intercalados en la Granja y Jardín de la Universidad de California en Santa Cruz. Foto de Jim Leap.
Especie/variedad del cultivo
La susceptibilidad a la alimentación de los sinfílidos de jardín puede variar considerablemente entre las distintas especies y variedades de plantas. En la mayoría de los casos, la tolerancia a la alimentación parece deberse a un mayor vigor y/o a una mayor producción de raíces (por ejemplo, brócoli, maíz) (Umble y Fisher, 2003a; Simigrai y Berry, 1974). En algunos casos, los sinfilanos de jardín pueden simplemente comer menos de ciertos cultivos o variedades, aunque esto no se ha demostrado experimentalmente. En general, los cultivos de semillas más pequeñas tienden a ser más susceptibles que los de semillas más grandes (Umble y Fisher, 2003a). Entre los cultivos que suelen sufrir daños se incluyen el brócoli y otras coles, las espinacas, la remolacha, la cebolla y la calabaza.
Las judías y las patatas rara vez sufren daños, incluso con densidades elevadas. Los cultivos perennes, como las fresas, las frambuesas, el lúpulo y los árboles de raíz desnuda (producción de vivero), también pueden sufrir daños, sobre todo durante la fase de establecimiento. Dentro de una misma especie, como el brócoli, algunas variedades son más tolerantes a los sinfílidos de jardín que otras (Simigrai y Berry, 1974).

Los cultivos perennes también pueden sufrir daños si hay sinfílidos presentes, como es el caso de estos arándanos.

Daños en los álamos híbridos.
Fase de crecimiento
Dentro de un mismo cultivo, la susceptibilidad suele estar relacionada con la fase de desarrollo del mismo. Por ejemplo, dentro de una variedad de tomate, los tomates sembrados directamente son más susceptibles que los plantones de cuatro semanas, los cuales a su vez son más susceptibles que los plantones de doce semanas. El uso de plantones o el aumento de su tamaño para reducir el daño causado por el
no resulta eficaz en todos los cultivos. Los plantones de brócoli y berenjena, por ejemplo, a menudo no logran arraigar cuando hay altas poblaciones de simfílidos en el huerto.
Densidad de plantas
Los sinfílidos de jardín no recorren grandes distancias por la superficie del suelo, como hacen los escarabajos de tierra. Sin embargo, son bastante activos y sorprendentemente ágiles para su tamaño, desplazándose tanto vertical como horizontalmente a través del perfil del suelo. Esto resulta especialmente evidente cuando, por ejemplo, las plántulas trasplantadas a un semillero ya preparado en el que aparentemente hay pocos sinfílidos de jardín se ven invadidas por estos insectos, que se arrastran por todas sus raíces menos de un día después de la plantación.
El número de sinfílidos de jardín que se alimentan de cada planta en una zona concreta (por ejemplo, un bancal elevado) depende, en parte, del número de plantas presentes en ese bancal. En algunos casos, aumentar la densidad de plantas —lo cual, por supuesto, debe sopesarse teniendo en cuenta la competencia entre ellas— da lugar a una mayor producción. Entre las variaciones de esta estrategia se encuentra la siembra de un cultivo «de distracción» o «de dilución» temprano en un bancal o junto a una hilera de cultivo.
Un buen cultivo de dilución es un cultivo de bajo coste, vigoroso y fácil de establecer (por ejemplo, el pasto sudán en condiciones adecuadas) que aumenta la masa radicular en el suelo y «diluye» eficazmente a los sinfílidos del huerto lo suficiente como para que el cultivo objetivo se establezca. A medida que el cultivo objetivo se establece, se retira el cultivo de dilución.
Estrategias para reducir el acceso de los sinfílidos de jardín a las raíces de los cultivos
Dado que los sinfílidos de jardín no son capaces de excavar en el suelo, sino que dependen de los poros del suelo y de los canales creados por las raíces y otros organismos del suelo, su acceso a las raíces está estrechamente relacionado con la estructura del suelo, la densidad aparente («esponjosidad») del suelo y la conectividad de los poros. En general, las siguientes estrategias se centran en reducir temporalmente el número de sinfílidos de jardín en la capa superficial del suelo antes de la siembra, lo que permite que los cultivos se establezcan mientras el número de sinfílidos de jardín es bajo.
Labranza
Además de eliminar directamente a los sinfílidos de jardín, el laboreo desintegra los agregados del suelo, modificando los poros del suelo y su conectividad. Los efectos del laboreo varían según los tipos de implementos utilizados. En general, cuanto más disruptivo es el laboreo, mayor es el efecto que tendrá sobre los sinfílidos de jardín. El arado o el discado, seguidos de una preparación minuciosa de un lecho de siembra fino con un motocultor o una roterra, suelen reducir las poblaciones de sinfílidos de jardín que se alimentan en la superficie durante dos o tres semanas. Durante este periodo, se forman poros a medida que se produce cierta agregación, y las lombrices y las raíces de las plantas crean nuevos canales a través del suelo. Una alteración menos intensa del suelo, como la excavación manual o el cultivo superficial con una grada o un cultivador de franjas, puede tener
un efecto significativamente menos disruptivo sobre los sinfílidos de jardín.

Plantas que crecen en el suelo compactado por las huellas de los neumáticos en un campo que, por lo demás, está desnudo e infestado de sinfilanos.
Compactación/Camas elevadas
La protección de las raíces de las plantas frente a los sinfílidos del jardín se hace evidente a veces en zonas donde los neumáticos de los tractores han compactado el suelo, o en áreas donde un motocultor o un arado de discos ha formado una capa compactada o «capa de arado».
Aunque la compactación puede tener algunos efectos negativos, en algunos suelos es posible compactarlos de forma beneficiosa utilizando, por ejemplo, un rodillo de jardinería, lo que reduce el movimiento de los simfílidos del jardín lo suficiente como para permitir que las plantas se establezcan. A menudo se dan las condiciones opuestas en los bancales elevados con un alto contenido de materia orgánica, donde el suelo tiene una densidad aparente muy baja y los simfílidos del jardín pueden moverse libremente por todo el bancal.
Referencias
Berry, R. E. 1972. Sinfílano de jardín: reproducción y desarrollo en el laboratorio. (Scutigerella immaculata). Journal of Economic Entomology. Vol. 65. p. 1628-1632.
Berry, R. E. 1973. Biología del ácaro depredador Pergamasus quisquiliarum sobre el sinfílido de jardín Scutigerella immaculata en condiciones de laboratorio. Ann. Entomol. Soc. Am. 66: 1354-1356.
Berry, R. E. y R. R. Robinson. 1974. Biología y control del sinfílano de jardín. Universidad Estatal de Oregón. Servicio de Extensión. Circular de Extensión n.º 845.
Edwards, C. A. 1957. «Técnicas sencillas para la cría de colémbolos, sinfilos y otros pequeños artrópodos del suelo», pp. 412-416. En D. K. M. Kevan [ed.], Zoología del suelo. Butterworths Publications Ltd., Londres.
Edwards, C. A. 1958. La ecología de los simfilos: parte I. Poblaciones. Entomologia Experimentalis et Applicata 1: 308-319.
Edwards, C. A. 1959a. Claves para la identificación de los géneros de los Symphyla. Journal of the Linnean Society XLIV: 164-169.
Edwards, C. A. 1959b. La ecología de los simfilos: parte II. Migraciones estacionales en el suelo. Entomologia Experimentalis et Applicata 2: 257-267.
Edwards, C. A. 1961. La ecología de los sinfilos: parte III. Factores que determinan su distribución en el suelo. Entomologia Experimentalis et Applicata 4: 239-256.
Edwards, C. A. 1990. Symphyla, pp. 891-910. En D. L. Dindal [ed.], Soil biology guide. Wiley, Nueva York.
Edwards, C. A. y E. B. Dennis. 1962. «El muestreo y la extracción de sinfílidos del suelo», pp. 300-304. En P. W. Murphy [ed.], *Progress in Soil Zoology*. Butterworths, Londres.
Eltoum, E. M. A. y R. E. Berry. 1985. Influencia de los daños causados por el simfílido de jardín (Symphyla: Scutigerellidae) en las raíces sobre los procesos fisiológicos de las judías verdes. Environ. Entomol. 14: 408-412.
Filinger, G. A. 1928. Observaciones sobre los hábitos y el control del ciempiés de jardín, Scutigerella immaculata, Newport, una plaga en los invernaderos. J. Econ. Entomol. 2: 357-360.
Filinger, G. A. 1931. El sinfílido de jardín. Boletín 486 de la Estación Experimental Agrícola de Ohio: 1-33.
Getzin, L. W. y C. H. Shanks. 1964. Infección del sinfilido de jardín, Scutigerella immaculata (Newport), por Entomophthora coronata (Constantin) Kevorkian y Metarrhizium anisopliae (Metchnikoff) Sorokin. J. Insect Path. 6: 542-543.
Gould, G. E. y C. A. Edwards. 1968. Daños causados al maíz de campo por los sinfílidos. Actas de la Academia de Ciencias de Indiana 77: 214-221.
Howitt, A. J. 1959. Control de Scutigerella immaculata (Newport) en la costa noroeste del Pacífico mediante fumigantes del suelo. J. Econ. Entomol. 52: 678-683.
Howitt, A. J. y R. M. Bullock. 1955. Control del ciempiés de jardín. J. Econ. Entomol. 48: 246-250.
Illingworth, J. F. 1927. «Symphylids destructivos para las raíces de la piña». *Pineapple News*, marzo-diciembre: 88-91.
Koontz, F. R. 1968. Relaciones biológicas y ecológicas entre el hongo Entomophthora coronata (Constantin) Kevorkian y el sinfilano de jardín
Scutigerella immaculata (Newport). Tesis doctoral, Universidad Estatal de Oregón, Corvallis.
Martin, C. H. 1948. Movimiento y poblaciones estacionales del ciempiés de jardín en el suelo de los invernaderos. J. Econ. Entomol. 41: 707-715.
Michelbacher, A. E. 1935. La situación económica del ciempiés de jardín, Scutigerella immaculata (Newp.), en California. J. Econ. Entomol. 28: 1015-1018.
Michelbacher, A. E. 1938. La biología del ciempiés de jardín Scutigerella immaculata. Hilgardia 11: 55-148.
Michelbacher, A. E. 1939. Variación estacional en la distribución de dos especies de Symphyla de California. J. Econ. Entomol 32: 53-57.
Michelbacher, A. E. 1949. La ecología de los simfilos. The Pan-Pacific Entomologist 25: 1-12.
Peachey, E., A. Moldenke, R. D. William, R. Berry, E. Ingham y E. Groth. 2002. Efecto de los cultivos de cobertura y del sistema de labranza sobre los sinfilos (Symphyla: Scutigerella immaculata) y otros organismos del suelo en suelos agrícolas. Appl. Soil Ecol. 21: 59-70.
Riley, H. K. 1929. El ciempiés de los invernaderos. Boletín 331 de la Estación Experimental Agrícola de Indiana: 1-14.
Scheller, U. 1986. Symphyla de Estados Unidos y México. Monografía espeleológica n.º 1 del Museo de Texas: 87-125.
Sechriest, R. E. 1972. Control del sinfílano de jardín en los campos de maíz de Illinois. J. Econ. Entomol. 65: 599-600.
Shanks, C. H. 1966. Factores que influyen en la reproducción del sinfílido de jardín Scutigerella immaculata. J. Econ. Entomol. 59: 1403-1406.
Simigrai, M. y R. E. Berry. 1974. Resistencia del brócoli al simfílido de los huertos. J. Econ. Entomol. 67: 371-373.
Stimmann, M. W. 1968. Efecto de la temperatura sobre la infección del sinfílano de jardín por Entomophthora coronata. J. Econ. Entomol 61: 1558-1560.
Swenson, K. G. 1965. Infección del sinfílano de jardín, Scutigerella immaculata, por el nematodo DD-136. J. Invert. Path. 8: 133-134.
Umble, J. R., y J. R. Fisher. 2003a. Influencia de la alimentación subterránea de los sinfílidos de jardín (Cephalostigmata: Scutigerellidae) en la salud de las plantas. Environmental Entomology 32: 1251-1261.
Umble, J. R., y J. R. Fisher. 2003b. Consideraciones sobre el muestreo de los sinfílidos de jardín, Scutigerella immaculata Newport, en el oeste de Oregón. Journal of Economic Entomology 96: 969-974.
Umble, J. R., y J. R. Fisher. 2003c. Idoneidad de determinados cultivos y suelos para el desarrollo de la población del simfílido de jardín (Symphyla, Scutigerellidae: Scutigerella immaculata Newport). Journal of Applied Soil Ecology 24: 151-163.
Waterhouse, J. S. 1969. Evaluación de un nuevo ciempiés depredador, Lamyctes sp., sobre el sinfílido de jardín Scutigerella immaculata. Can. Entomol. 101: 1081-1083.
Waterhouse, J. S., R. Seymour y E. W. Rutkowski. 1969. Efectos biológicos de la inanición en el sinfílano de jardín. J. Econ. Entomol. 62: 338-341.
Woodworth, C. W. 1905. Un nuevo ciempiés de importancia económica. Calif. J. Tech. 6: 38-42.
Wymore, F. H. 1931. El ciempiés de jardín. Boletín de la Estación Experimental de California n.º 518: 1-22.
Symphylans: Opciones para el control de plagas del suelo
Por Jon Umble, Universidad Estatal de Oregón; Rex Dufour, NCAT; Glenn Fisher, Universidad Estatal de Oregón; James Fisher, USDA/ARS; Jim Leap, Universidad de California, Santa Cruz; Mark Van Horn, Universidad de California, Davis
©NCAT
Publicado en febrero de 2006
IP283
Esta publicación ha sido elaborada por el Centro Nacional de Tecnología Apropiada (NCAT) a través del programa de Agricultura Sostenible de ATTRA, en el marco de un acuerdo de cooperación con el Departamento de Desarrollo Rural del Departamento de Agricultura de los Estados Unidos (USDA). Su elaboración también ha sido posible, en parte, gracias a la financiación procedente de una subvención para investigación y educación del programa de Investigación y Educación en Agricultura Sostenible del Oeste (Western SARE) del USDA. ATTRA.NCAT.ORG.
Fotografías de John Umble, salvo que se indique lo contrario.
